抗体药物偶联物(ADC)由抗体、连接子和细胞毒性药物组成,可利用单克隆抗体(mAbs)的特异性,选择性地向表达抗原的肿瘤细胞投递有效的细胞毒性药物,被业内誉为“魔法子弹”。

ADC实现了对肿瘤的“精确制导”,改变了肿瘤的治疗格局。虽疗效喜人,但不良反应是任何药物不可避免的“另一面”。处理不当不仅拖治疗进度的“后腿”,还会影响患者的预后和生活质量。日前,广州复大肿瘤医院药学部潘燕在“复大新视野 徐克成大讲堂”第82讲上与大家分享关于ADC药物的概述及其不良反应。
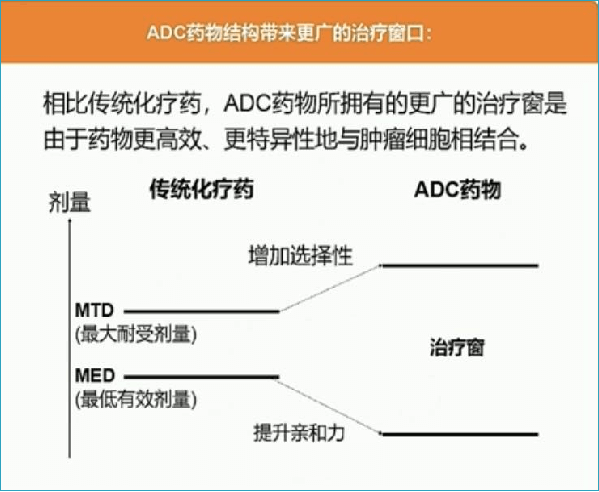
ADC药物具有可同时克服传统化疗及靶向治疗的局限性的优势,能特异性识别目标癌细胞,通过破坏DNA、微管蛋白等阻止细胞分裂,起到杀死癌细胞的作用。
其作用机制主要分为5步:
1、注射进体内的ADC与靶细胞抗原结合;
1、注射进体内的ADC与靶细胞抗原结合;
2、ADC-抗原复合物内吞作用进入细胞;
3、ADC药物裂解,细胞毒药物释放至胞质,通过破坏DNA或抑制微管聚合发挥作用;
4、靶细胞凋亡,当目标细胞死亡时,活跃的细胞毒素小分子也可能杀死周围的肿瘤细胞(旁观者效应);
5、连接子的稳定性、细胞毒素的性质(如极性大小)等决定ADC是否有旁观者效应。
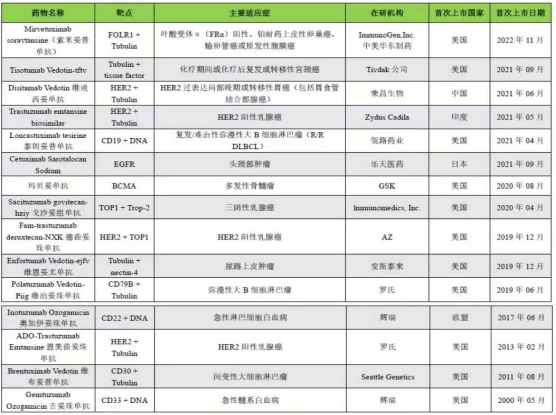
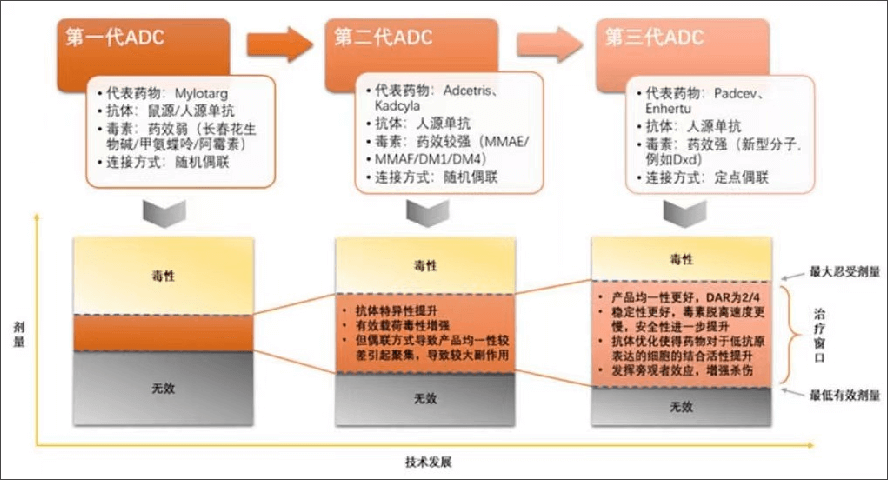
由于抗体和细胞毒性药物不同,不同ADC药物的不良反应也不同。常见的不良反应包括血液学不良反应,输液反应,消化道反应,周围神经病变,肝、肺和心脏毒性等。
《中国乳腺癌抗体药物偶联物安全性管理专家共识》将ADC不良反应分为“需要特殊关注”和“常见”两类。其中,需要特殊关注的不良反应主要包括血小板降低和间质性肺病。
血小板降低
指基于实验室监测结果,血液样本中的血小板数量减少,是乳腺癌治疗常见的不良反应。
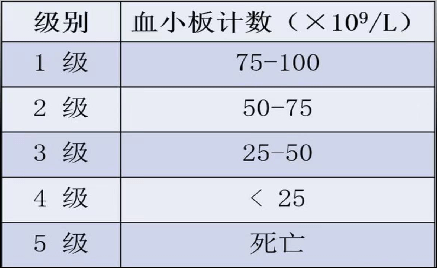
▲CTCAE 5.0版本-- 血小板减少严重程度分级

▲FEC:F 氟尿嘧啶 E 表柔比星 C 环磷酰胺
不同药物引起血小板减少的机制也有区别:
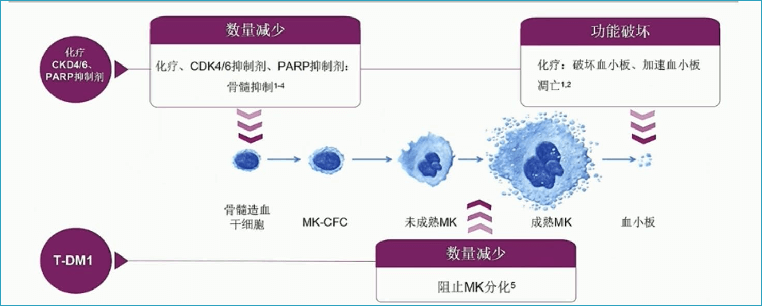
其中,T-DM1引起的血小板减少多为1级或2级,3级及以上通常无症状且可管控。血小板降低呈现周期性规律,在下一次用药前可恢复至基本正常水平;或经过适当的剂量调整也可恢复,因此,大多患者可继续治疗。基于《共识》,将 ADC 治疗相关血小板减少的常规对症处理流程总结如下:
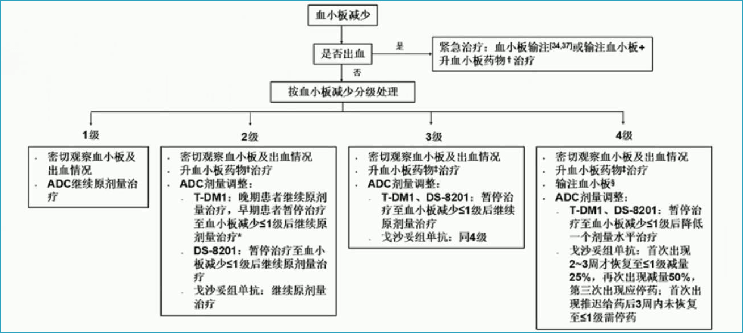
在ADC治疗期间,应常规监测血小板计数。若出现血小板减少,应及时按说明书调整剂量或停药。有指征时可以考虑输注血小板、升血小板药物等作为支持治疗。必要时请血液科会诊。
早期患者如因血小板减少需延迟2次给药,应考虑降低一个剂量水平再继续治疗;
升血小板药物:rhIL-11、rhTPO、TPO-RA;
输注血小板:如<10×109/L,或<20×109/L且伴发热。
此外,2018 年《ASCO临床实践指南》提出,对于实体瘤患者,当血小板<10×109/L时,需预防性输注血小板;更高阈值的血小板输注适用于有局部活动性出血的情况,可见于坏死性肿瘤患者。2019 年《中国肿瘤化疗相关性血小板减少症专家共识》认为,当WHO出血分级≥2级,推荐输注血小板;0-1级且血小板计数达到预防性输注指征的患者,也可输注血小板。
间质性肺炎
DS-8201-A-J101的I期临床研究纳入118例既往使用T-DM1治疗的HER2阳性乳腺癌患者,在使用至少一剂建议扩大剂量的DS-8201a(T-DXd)中发现20例(16.9%)患者出现和药物相关的ILD/肺炎,其中1例发生3级 AEs,2例出现与治疗相关的肺炎死亡。
DESTINY-Breast01的Ⅱ期临床研究报道了184例T-DM1耐药/难治的HER2阳性不可切除和/或转移性乳腺癌患者,推荐剂量的DS-8201a治疗。其中25例(13.6%)患者出现治疗相关的ILD,其中2.7%发生≥3级事件,4例患者死于和治疗相关的肺炎。
基于《共识》,在DS-8201和T-DM1治疗期间,应监测并及时评估呼吸道症状和体征,并告知患者可能的风险以及出现症状后立即报告的必要性;一旦疑诊ILD/肺炎,应严格进行剂量调整或终止用药,并考虑立即开始糖皮质激素治疗,同时请呼吸科会诊以确认方案。总结ADC治疗相关ILD/肺炎的常规对症处理流程如下: