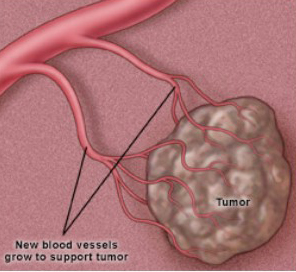
全身化疗时,化疗药物全身分布,肿瘤组织内药物浓度低,经常达不到足够的肿瘤细胞杀伤力,而全身其他脏器内药物分布不可忽视。因此,全身副作用大,而肿瘤组织内杀伤力不满意。为此,人们常改用介入法动脉灌注给药。将导管插入到肿瘤组织附近的供血动脉内,直接动脉灌注给药。这样,肿瘤区化疗药瞬间浓度大大提高,但缺点是药物很快随血液向全身流走,达不到高浓度化疗药持续发挥作用。
肿瘤癌血管介入疗法(Cancer Vascular Intervention, CVI)是采用特殊工艺,将多种化疗药物配成微小颗粒,再按介入法超选择插管到肿瘤供血动脉内给药。这种化疗药物微小颗粒将选择性地渗透到肿瘤组织内并保持长时间高浓度。其原理是:肿瘤毛细血管内皮细胞间有很多缝隙,而正常毛细血管内皮细胞间是紧密连接的。这样,介入法超选插管注入的化疗药微小颗粒渗透到肿瘤组织间隙内,引起组织渗透压增高,压迫肿瘤毛细血管选择性闭塞,从而使化疗药物较长时间滞留于肿瘤组织内。而到达正常毛细血管内的化疗药则由于颗粒过小,不会引起毛细血管栓塞,随血流流走,加之化疗药用量极微,故不会对正常组织产生过多损伤,全身副作用非常小。
一、从根源直击病灶,杀伤实体肿瘤
第一步:导管注入微粒药物和栓塞剂
在影像设备导向下,将导管通过动脉插入病灶血管通道,将抗癌药物和栓塞剂有机结合,一起注入靶动脉。
第二步:阻断肿瘤细胞营养供给
栓塞剂堵塞肿瘤供血血管,切断肿瘤营养供应,超微粒药物停留在肿瘤内,迅速发挥作用消灭肿瘤。

第三步:肿瘤细胞“饥饿死亡”
肿瘤内部药物浓度较高,肿瘤细胞在被“毒害”的基础上再遭受 “饥饿”的打击,直至消亡。
二、解读癌血管介入治疗在临床上的广泛应用
作用1:切断肿瘤细胞营养供给,延缓生长
大部分恶性肿瘤患者一旦确诊就已为中晚期,极易扩散转移;介入治疗可有效控制病情发展。
作用2:缩小瘤体,为手术切除创造条件
绝大多数的恶性肿瘤患者常常到了中晚期,错失切除机会。介入治疗可快速缩小瘤体。
作用3:损伤小,药物直达病灶降低毒副作用
传统放化疗不分敌我、杀伤力极大。肿瘤患者到了中晚期,身体虚弱,更加不能使用“摧残性”手段,微创可有效解决。
作用4:靶点导向“杀死”肿瘤细胞,减少转移
转移是癌症区别于其他疾病的特征,也是大部分患者死亡的真正原因。微创介入靶点导向作用,切断肿瘤血液供应,将肿瘤细胞饿死,有效控制转移。
三、癌血管介入治疗适应症
针对早、中、晚期各期实体肿瘤的患者,以及不愿意或不适合手术、放疗、化疗的患者进行根治性微创治疗。
微创介入治疗可解决许多难题,再结合严谨的中药治疗、免疫治疗等综合治疗技术可获得满意疗效。
四、癌血管介入治疗病例
病例1 肺癌
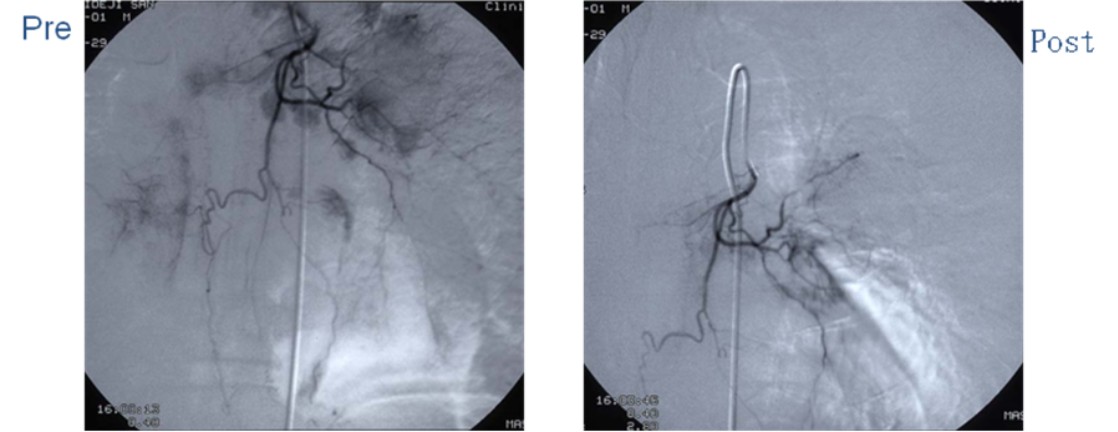
A 治疗前DSA造影支气管动脉 B 化疗药关注后立刻造影,瘤血管明显减少
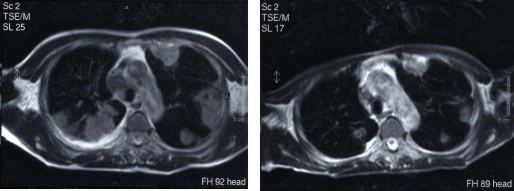
C治疗前MRI片示双肺内多发病灶 D 治疗1月后查病灶明显减少
病例2 乳腺癌肝转移
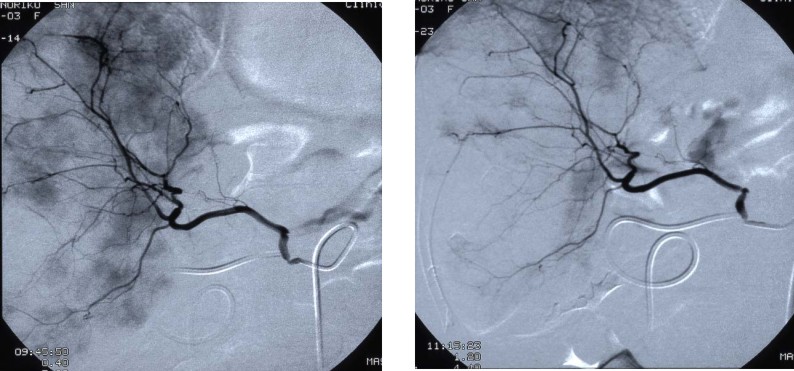
A 治疗前DSA示肝内广泛瘤染色 B 癌血管介入治疗后立刻造影示染色早明显减少
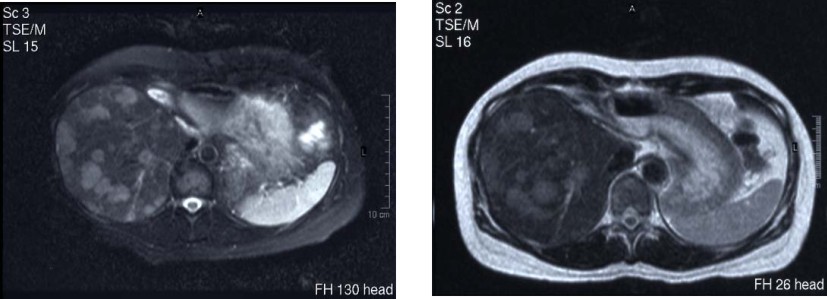
C 治疗前MRI示肝内广泛病灶 D 治疗3月病灶减少
病例3 乳腺癌骨转移
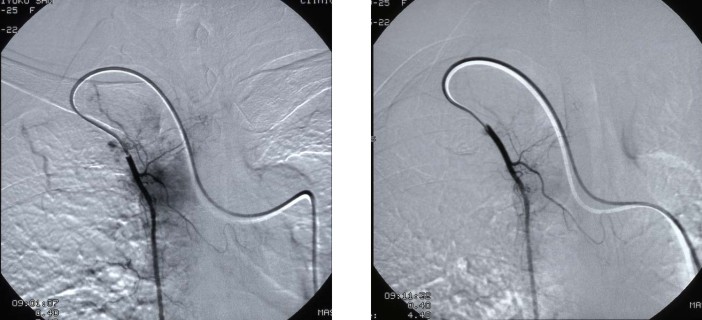
A 治疗前DSA造影见胸骨区瘤染色 B CMI化疗药物治疗后立刻造影见瘤染色明显减轻

C 治疗前MRI显示胸骨病灶 D 治疗后转移灶消失
病例4 乳腺癌 stage IIIA
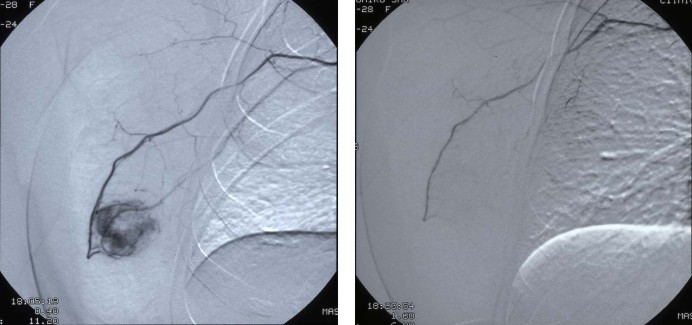
A 治疗前DSA示乳腺病灶 B 癌血管介入后立即造影瘤染色消失

C 治疗前DSA D 治疗后3个月见病灶消失
病例5 结肠癌
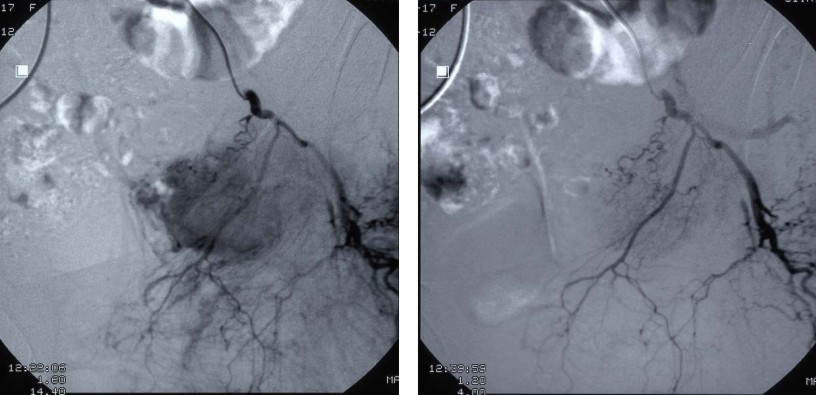
A 治疗前DSA B 灌注CMI化疗药物立即造影瘤染色明显减少
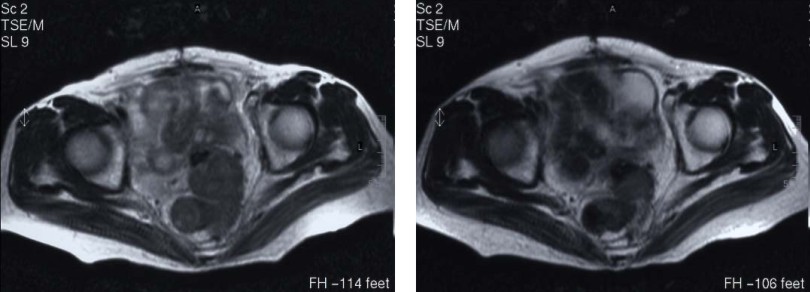
C 治疗前MRI见乙状结肠病灶 D 治疗后病灶缩小